
Clo là gì? Tính chất lý hóa, Ứng dụng, Tác động đối với sức khỏe
Clo là gì? Đây là câu hỏi được nhiều người quan tâm. Chúng ta ít nhất đã biết được chất này ứng dụng trong đời sống. Tuy nhiên, có nhiều người vẫn chưa hiểu rõ đặc điểm và tính chất của chúng. Trong bài viết này, hãy cùng Vietchem tìm hiểu về khái niệm clo và những ứng dụng của chúng trong đời sống nhé.
1. Clo là gì?
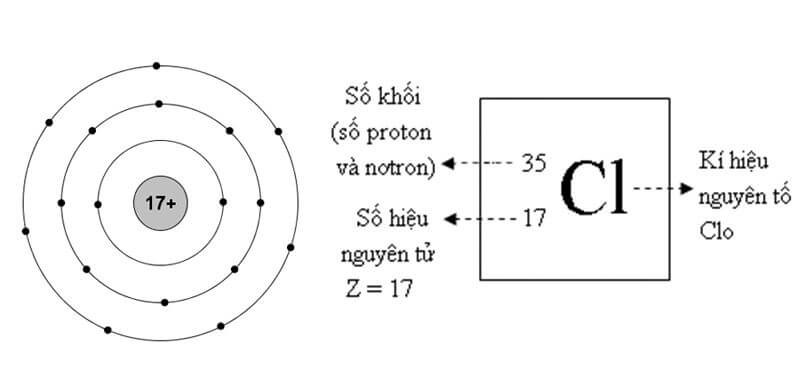
Clo hay Chlorine là nguyên tố hóa học trong bảng tuần hoàn nguyên tố có ký hiệu Cl và thuộc chu kì 3 của bảng tuần hoàn. Clo có ái lực điện tử cao nhất và có độ âm điện đứng thứ 3 trong tất cả các nguyên tố. Clo tồn tại ở 2 dạng đó là dạng lỏng và dạng khí.

Hình 1: Clo là một nguyên tố hóa học quan trọng
2. Tính chất vật lý của Clo
Clo có trạng thái khí, có màu vàng lục và mùi của clo vô cùng hắc trong điều kiện thường. Đây là một chất vô cùng độc hại.
Khi Clo ở dạng phân tử, Clo có khối lượng =71, chính vì vậy, Cl nặng hơn nhiều so với không khí. Khí clo tan vừa phải trong nước tạo thành nước clo có màu vàng nhạt và tan nhiều trong các dung môi hữu cơ.
Khí Clo là một khí có khả năng phản ứng ngay lập tức gần như với mọi nguyên tố. Ở 10 độ C một lít nước sẽ hòa tan được 3,10 lít clo và ở 30 độ C chỉ là 1,77 lít.
3. Tính chất hoá học của Clo
Clo là một phi kim nên có khả năng oxi hóa vô cùng mạnh. Trong các hợp chất, Clo thường có mức oxi hóa -1, trong hợp chất với F hoặc O các mức oxi hóa của Clo thường là +1, +3, +5 hay +7. Ngoài ra, trong một số trường hợp Clo có tính khử.
Khi Clo tác dụng với kim loại chúng sẽ tạo ra muối và tên muối này là halogenua. Đặc biệt, clo có thể tác dụng hầu hết với toàn bộ kim loại, ngoại trừ Au và Pt.
3.1. Clo tác dụng với nước
Phương trình phản ứng Clo tác dụng với nước sẽ tạo ra HCl và HClO, đây được gọi là phản ứng 2 chiều.
H2O + Cl2 => HCl + HClO.
Trong phản ứng clo với nước Clo là chất oxi hóa vừa là chất khử. Chi tiết như sau: Clo sẽ bị oxy hóa thành nguyên tử Cl-1 (HCl) và khử thành 1 nguyên tử Cl+1 (HClO). Mặt khác, trong dung dịch hay ở dạng ngậm nước, axit hipoclorơ (HClO) bị phân giải riêng biệt thành anion hypoclorit OCl−:
HClO ⇌ OCl- + H+
Dung dịch hỗn hợp của các chất Hcl dư, axit HCl, HClO còn được gọi là nước Clo.
3.2. Clo tác dụng với natri hidroxit
Clo tác dụng với dung dịch kiềm, khi tác dụng với NaOH loãng, nguội tạo ra javen. Cụ thể, ta có phản ứng:
Cl2 + 2NaOH -> NaCl + NaClO + H2O
Nước javen là hỗn hợp hai muối natri clorua (NaCl) và natri hypoclorit (NaClO).
3.3. Clo tác dụng với kim loại
Khi Clo tác dụng với kim loại chúng sẽ tạo ra muối và tên muối này là halogenua. Đặc biệt, clo có thể tác dụng hầu hết với toàn bộ kim loại, ngoại trừ Au và Pt.
2Fe +3Cl2 -> 2FeCl3
Hình 2: Các tính chất hóa học của Clo
4. Điều chế Clo
4.1. Phương pháp điều chế Clo trong phòng thí nghiệm
Đun nóng nhẹ dung dịch axit HCl đậm đặc với chất có khả năng oxy hóa mạnh như mangan dioxit (MnO2).
Phương trình phản ứng xảy ra như sau:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Nếu muốn thu được khí Clo tinh khiết, cần tiếp tục thực hiện các bước sau:
- Cho khí Clo qua bình axit sunfuric đặc, nó sẽ được làm khô nước.
- Thu khí Clo bằng phương pháp đẩy không khí do khí Clo nặng hơn không khí.
- Sử dụng bông tẩm xút, tránh khí Clo bay ra bên ngoài vì Clo là khí độc
Ngoài MNO2 có thể dùng một số chất oxy hóa khác như kali pemanganat (KMnO4), Kali Clorat (KClO3), Clorua vôi (CaOCl2).c
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O + 5Cl2
KClO3 + 6HCl → KCl + 3H2O + 3Cl2
CaOCl2 + 2HCl → Cl2 + CaCl2 + H2O
4.2. Điều chế khí Clo trong công nghiệp
Các nhà sản xuất tiến hành điện phân muối Natri Clorua bằng điện phân nóng chảy theo phương trình phản ứng:
2NaCl → 2Na + Cl2
Hoặc điện phân có màng ngăn dung dịch muối halogenua (natri clorua)
2NaCl + 2H2O → H2 + 2NaOH + Cl2
5. Clo dùng để làm gì?
Clo có nhiều ứng dụng trong sinh hoạt và sản xuất như:
- Clo được biết đến chủ yếu trong điều chế nhựa PVC cũng như các chất dẻo hay cao su
- Clo có tác dụng khử trùng.Chủ yếu dùng khí Clo là phổ biến nhất. Khi dùng trong xử lý nước, dưới môi trường áp suất cao và làm lạnh, Clo được chuyển hóa ở dạng lỏng
- Người ta sử dụng khí Clo ở dạng axit hipoclorơ HClO để khử trùng trong hồ bơi, hệ thống cấp nước, xử lý nước thải.
- Clo được dùng trong quá trình sản xuất giấy, thuốc nhuộm, thuốc trừ sâu, sơn… và nhiều đồ vật sử dụng hàng ngày khác.
- Ngoài ra, nó là nguyên liệu để sản xuất nhiều hợp chất hữu cơ và vô cơ.

Hình 3: Clo có nhiều ứng dụng trong sản xuất và sinh hoạt
6. Clo có độc không?
Bên cạnh những ứng dụng của Clo thì nó được biết đến như một chất độc. Sau đây là những tác hại của clo:
- Clo rất có hại cho sức khỏe con người. Clo bất luận ở dạng khí hay lỏng cũng có thể là nguyên nhân gây tổn thương vĩnh viễn, đặc biệt hơn là có thể gây tử vong. Clo tiềm ẩn của sự xuất hiện bệnh về cổ họng, mũi và đường hô hấp (đường thực quản gần phổi). Hậu quả nghiêm trọng trong giai đoạn ngắn
- Ảnh hưởng của mật độ 250 ppm cho 30 phút có thể gây tử vong cho người lớn
- Sự kích thích cao xuất hiện khí, khi hít vào có thể làm bỏng da và mắt.
- Hậu quả của bệnh mãn tính sẽ phần nào gây chết người trong thời gian dài: Đối với tác động lâu dài của khí Clo, sẽ làm cho người ta trở nên già trước tuổi, gây ra những vấn đề về phế quản, sự ăn mòn của răng, các bệnh liên quan đến phổi như lao.
- Theo nghiên cứu, phụ nữ mang thai sử dụng nước chứa clo có nguy cơ gây sảy thai, dị tật.

Hình 4: Nếu không sử dụng đúng cách, Clo có thể gây hại
7. Cách xử lý clo dư thừa trong nước hiệu quả
Sử dụng than hoạt tính: Than hoạt tính có khả năng hấp thụ Clo bằng cách tương tác với bề mặt của nó. Các hợp chất cacbon trong than có thể tương tác với Clo và các hợp chất Clo để loại bỏ chúng khỏi nước. Loại than hoạt tính (GAC) thường được sử dụng trong các hệ thống lọc nước lớn để loại bỏ Clo.
Sử dụng tia cực tím: Ánh sáng cực tím có thể được sử dụng để giảm lượng Clo tự do và Chloramine bằng cách phân hủy chúng thành acid hydrochloric.
Sử dụng hóa chất: Sulfite, bisulfites, metabisulfites có thể được sử dụng để phản ứng với Clo và loại bỏ nó khỏi nước.
Oxy hóa nước: Cho nước tiếp xúc với không khí trong môi trường thoáng khí để giúp Clo bay hơi và thoát khỏi nước.
Sử dụng máy lọc công nghệ RO: Máy lọc nước thẩm thấu ngược (RO) có khả năng loại bỏ lên đến 99% Clo trong nước. Tuy nhiên, máy lọc này cũng có thể loại bỏ các khoáng chất tự nhiên, gây ra sự thiếu hụt dinh dưỡng khi sử dụng nước đã được lọc
8. Một số câu hỏi thường gặp
(1) Clo hóa trị mấy?
Clo có hóa trị I
(2) Clo nguyên tử khối là bao nhiêu?
Clo có nguyên tử khối là 35,453 u
(3) Clo là phi kim hay kim loại
Cl (Clo) trong bảng tuần hoàn hóa học nằm ở ô số 17. Đây là vị trí của nhóm các nguyên tố Halogen. Vì vậy tất cả các nguyên tố trong nhóm Halogen đều là nguyên tố phi kim
Như vậy là bạn vừa tìm hiểu xong khái niệm Clo là gì. Đây là một trong những chất được ứng dụng nhiều nhất trong sinh hoạt và sản xuất. Tuy nhiên, bạn cần tìm hiểu rõ những đặc tính của Clo để sử dụng phù hợp và tránh bị tổn hại khi dùng không đúng cách.
Link nội dung: https://iir.edu.vn/clo-la-gi-tinh-chat-ly-hoa-ung-dung-tac-dong-doi-voi-suc-khoe-a17827.html